- 나노기술로 재구조화된 5-Fu, 백혈병 세포 침투 12.5배 향상
- 동물 모델에서 암 진행 59배 지연, 생존 기간 대폭 연장
- 암 환자 삶의 질 향상 기대, 임상 시험 추진으로 의료 혁신 가속
 노스웨스턴 대학교 과학자들이 나노기술을 활용해 기존 항암제를 재설계함으로써 약효와 안전성을 획기적으로 개선했다. DNA에 결합하는 구형 핵산으로 약물을 재구성함으로써 연구팀은 약효가 약하고 용해도가 낮은 화합물을 백혈병 세포를 효과적으로 표적화하면서도 건강한 조직은 손상시키지 않는 정밀 암 치료제로 탈바꿈시켰다. [출처: Shutterstock; https://scitechdaily.com/new-drug-kills-cancer-20000x-more-effectively-with-no-detectable-side-effects/]
노스웨스턴 대학교 과학자들이 나노기술을 활용해 기존 항암제를 재설계함으로써 약효와 안전성을 획기적으로 개선했다. DNA에 결합하는 구형 핵산으로 약물을 재구성함으로써 연구팀은 약효가 약하고 용해도가 낮은 화합물을 백혈병 세포를 효과적으로 표적화하면서도 건강한 조직은 손상시키지 않는 정밀 암 치료제로 탈바꿈시켰다. [출처: Shutterstock; https://scitechdaily.com/new-drug-kills-cancer-20000x-more-effectively-with-no-detectable-side-effects/]
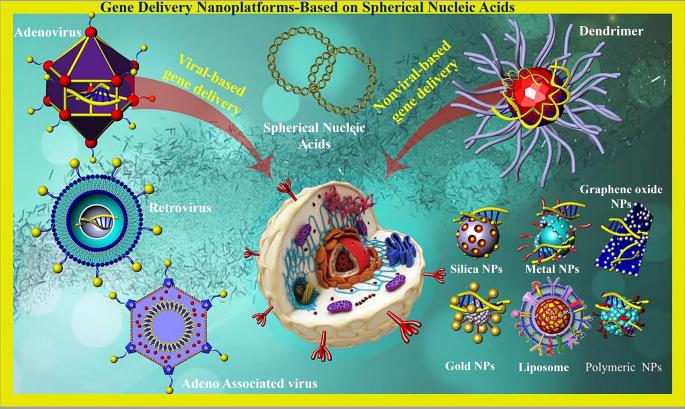
노스웨스턴 대학 연구팀이 전통적인 화학요법 약물인 5-플루오로우라실(5-Fu)을 나노기술로 재설계하여, 급성 골수성 백혈병(AML) 치료에서 획기적인 성과를 거두었다. 이 새로운 구형 핵산(SNA) 형태의 약물은 기존 약물의 용해도 문제를 해결하고, 암세포에 선택적으로 침투하여 파괴한다. 연구 리더인 채드 A. 미르킨 교수는 "동물 모델에서 종양 성장을 완전히 멈추는 결과를 보였다"고 밝혔다.
SNA 약물은 나노입자 코어에 DNA 또는 RNA 가닥을 둘러싸고, 여기에 5-Fu를 화학적으로 결합한 구조다. 이는 기존 5-Fu의 낮은 용해도(생체 유체에서 1% 미만 용해)와 비선택적 독성을 극복한다. 골수 세포에 과발현된 스캐빈저 수용체를 이용해 자연스럽게 세포 내부로 유입되며, 내부 효소가 DNA 껍질을 분해하여 약물을 방출한다. 실험 결과, 백혈병 세포에 12.5배 더 효율적으로 침투하고, 20,000배 더 효과적으로 파괴하며, 암 진행을 59배 느리게 만들었다. 혈액과 비장에서 백혈병 세포를 거의 완전히 제거했으며, 생쥐의 생존 기간을 크게 연장했다.
특히, 건강한 조직에 대한 부작용이 전혀 관찰되지 않아 기존 화학요법의 메스꺼움, 피로, 심부전 등의 문제를 해결할 수 있다. 미르킨 교수는 "대부분의 화학요법은 암세포와 건강 세포를 구분 없이 공격하지만, SNA는 골수 세포를 선택적으로 타겟팅한다"고 설명했다. 이 연구는 ACS Nano 저널에 게재되었으며, 국립암연구소와 국립당뇨병·소화기·신장질환연구소의 지원을 받았다.
향후 연구팀은 더 큰 동물 모델과 인간 임상 시험을 계획 중이다. 이 기술은 암뿐만 아니라 감염병, 신경퇴행성 질환, 자가면역 질환 치료에도 적용 가능하며, 이미 7개의 SNA 기반 요법이 임상 시험 중이다. 이 발견은 구조적 나노의학의 잠재력을 강조하며, 암 치료의 새로운 패러다임을 제시한다.
 AI 혁신 물결: xAI의 세계 모델, OpenAI GPT-5 업데이트, Hugging Face 오픈소스 NLP 모델 출시
2025년 말, AI 분야에서 주요 기업들의 연이은 발표가 이어지며 기술 발전의 속도가 가속화되고 있다. xAI의 로보틱스용 물리 세계 이해 모델 개발, OpenAI의 GPT-5 시리즈 업데이트, 그리고 Hugging Face의 맞춤형 NLP 오픈소스 모델 출시가 그 중심에 있다. 이러한 발전은 로보틱스, 자연어 처리, 콘텐츠 생성 등 다양한 영역에서 실용적 적용을 촉진할 ...
AI 혁신 물결: xAI의 세계 모델, OpenAI GPT-5 업데이트, Hugging Face 오픈소스 NLP 모델 출시
2025년 말, AI 분야에서 주요 기업들의 연이은 발표가 이어지며 기술 발전의 속도가 가속화되고 있다. xAI의 로보틱스용 물리 세계 이해 모델 개발, OpenAI의 GPT-5 시리즈 업데이트, 그리고 Hugging Face의 맞춤형 NLP 오픈소스 모델 출시가 그 중심에 있다. 이러한 발전은 로보틱스, 자연어 처리, 콘텐츠 생성 등 다양한 영역에서 실용적 적용을 촉진할 ...

 서울국제조각페스타 2026, 코엑스서 예술과 기업의 만남 성황
서울국제조각페스타 2026, 코엑스서 예술과 기업의 만남 성황
 [손현식 칼럼] 270만 외국인 시대, ‘함께 사는 법’은 배운 적이 없다
[손현식 칼럼] 270만 외국인 시대, ‘함께 사는 법’은 배운 적이 없다
 할리우드 배우노조, 스튜디오 측에 새 반대 제안 테이블에 올리다
할리우드 배우노조, 스튜디오 측에 새 반대 제안 테이블에 올리다
 하나님의 축복 속에서 시작된 사랑… 특별한 결혼의 여정
하나님의 축복 속에서 시작된 사랑… 특별한 결혼의 여정

 목록
목록